Nhấn ENTER để tìm kiếm hoặc ESC để đóng

Phần này dành riêng cho chuyên gia y tế. Tại đây, bạn có thể xem xét dữ liệu lâm sàng của NeuroAiD, đọc về dược lý của nó, xem qua các ấn phẩm và đánh giá mức độ phù hợp của NeuroAiD trong thực hành của bạn và đối với các bệnh nhân bị đột quỵ và chấn thương sọ não.
Để biết thêm thông tin, đừng ngần ngại liên hệ với chúng tôi qua email tại Medical@moleac.com
*Lưu ý: NeuroAiD™ (MLC601) là công thức ban đầu bao gồm 14 thành phần. NeuroAiD™ II và NurAiD™ II (MLC901) là công thức đơn giản hóa của NeuroAiD™ (MLC601) bao gồm 9 thành phần thảo mộc của công thức ban đầu. MLC901 và MLC601 đã được chứng minh là tương đương về mặt dược lý. Để đơn giản hóa, thông tin sau đây sẽ sử dụng NeuroAiD làm tên toàn cầu để chỉ định các sản phẩm trừ trường hợp đề cập cụ thể.
Theo quy định quốc gia ở mỗi quốc gia, NeuroAiD được đăng ký theo nhiều chương trình khác nhau, bao gồm thực phẩm bổ sung, thuốc truyền thống và thuốc thảo dược. Đến nay, NeuroAiD đã có mặt tại hơn 32 quốc gia trên toàn thế giới và không ngừng mở rộng phát triển.
Với sự hỗ trợ và tham gia của các nhà lãnh đạo quan điểm quốc tế về Thần kinh học và các nhà nghiên cứu giàu kinh nghiệm, NeuroAiD đã tập hợp hơn 45 ấn phẩm từ các nghiên cứu tiền lâm sàng đến các thử nghiệm lâm sàng ngẫu nhiên và nhằm giải quyết nhu cầu y tế trên toàn thế giới.

Liều dùng khuyến cáo là 2 viên mỗi lần, ngày 3 lần, dùng tối thiểu trong 3 tháng.
Đường uống với một ly nước. Đối với những người gặp khó khăn khi nuốt, có thể mở viên nang và pha loãng hàm lượng trong nước. Cũng có thể quản lý nội dung pha loãng qua ống thông dạ dày.
Cho đến nay, không có tương tác thuốc nào với NeuroAiD được báo cáo. Để biết thêm thông tin về hồ sơ an toàn của NeuroAiD, hãy nhấp vào ĐÂY.
Các thử nghiệm lâm sàng đã công bố đã xác nhận rằng NeuroAiD không có tác dụng làm loãng máu hoặc ảnh hưởng đến chức năng gan hoặc thận. Tương tự, NeuroAiD không có bất kỳ ảnh hưởng nào đến huyết áp và không gây ra bất kỳ thay đổi nào về các thông số về tim, huyết học, cầm máu và sinh hóa.1,2
Các thử nghiệm lâm sàng về NeuroAiD chỉ báo cáo một số trường hợp hiếm gặp về buồn nôn, nhức đầu nhẹ, khát nước nhiều hơn, khô miệng và nôn mửa đối với bệnh nhân dùng NeuroAiD. Trong những trường hợp này, nên giảm một nửa liều NeuroAiD trong vài ngày và tăng dần liều.
Việc sử dụng NeuroAiD ở phụ nữ mang thai, phụ nữ đang cho con bú và trẻ em không được ghi nhận và không được khuyến cáo. Cho đến nay, không có chống chỉ định nào khác được biết đến.
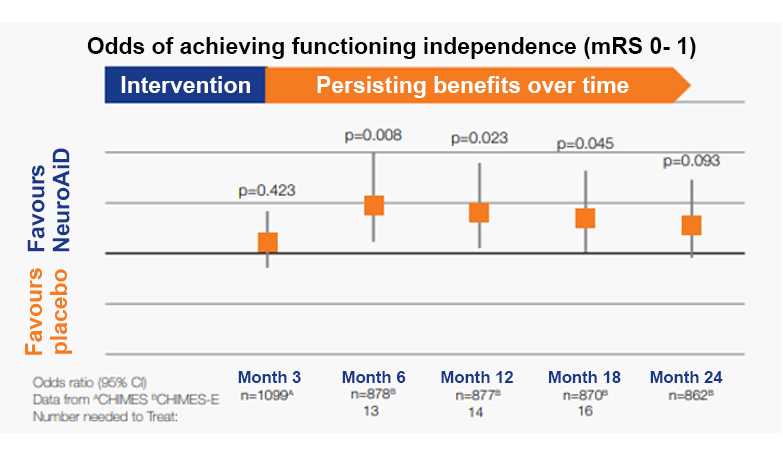
+50% khả năng đạt được sự độc lập về chức năng sau 6 tháng.
Phục hồi liên tục với các lợi ích quan sát được trong hơn 2 năm
*CHIMES-E được xuất bản trong tạp chí Bệnh mạch máu não là quá trình theo dõi kéo dài đến 24 tháng đã được lên kế hoạch trước của nghiên cứu CHIMES5, một nghiên cứu kéo dài 3 tháng được thực hiện trên 1099 đối tượng. Nghiên cứu CHIMES đã được công bố trên tạp chí Stroke vào năm 2013. **Các yếu tố tiên lượng được xác định là tuổi cao hơn, giới tính nữ, điểm NIHSS cơ bản ≥ 10 và thời gian dùng liều đầu tiên là 48 giờ.
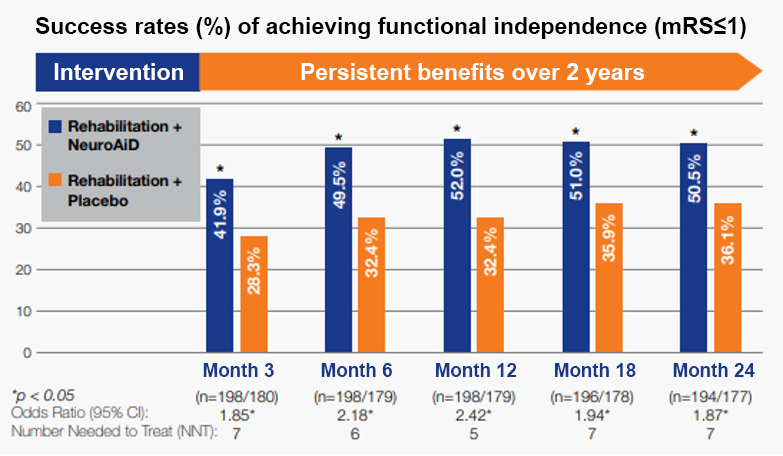
+50% khả năng đạt được sự độc lập về chức năng sau 6 tháng.
Phục hồi liên tục với các lợi ích quan sát được trong hơn 2 năm
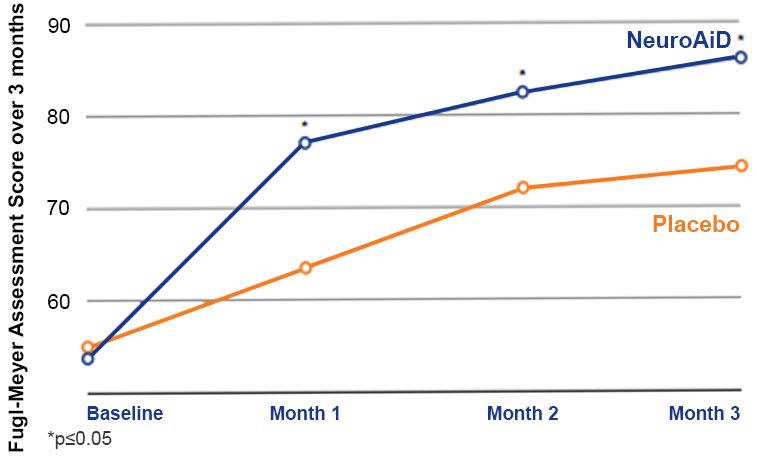
Phục hồi vận động tốt hơn đáng kể được quan sát kể từ tháng thứ nhất và duy trì đến tháng thứ ba.
References:
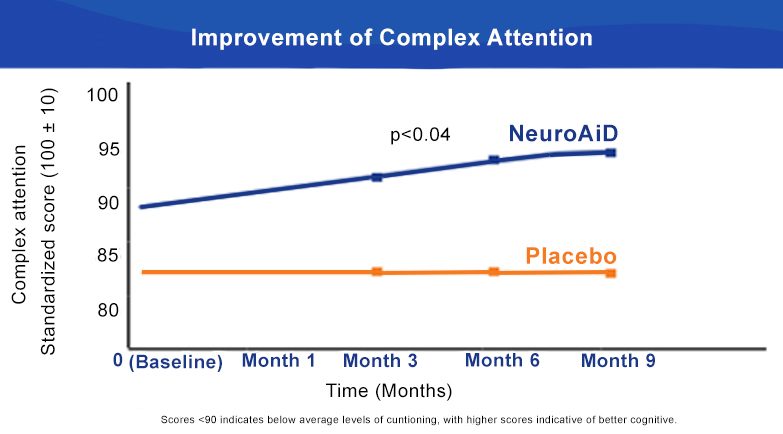
NeuroAiD cải thiện đáng kể Chức năng Điều hành và Chú ý Phức tạp sau 6 tháng.
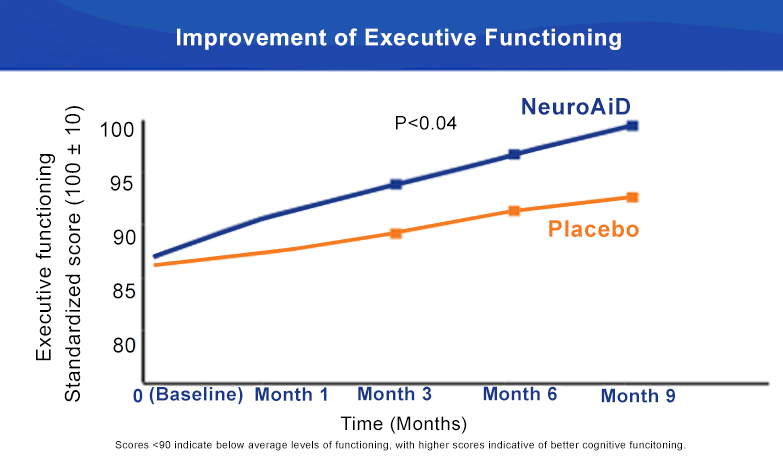
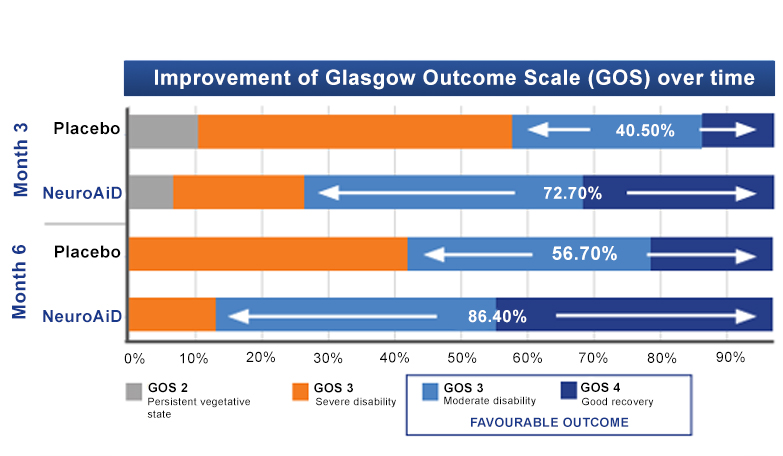
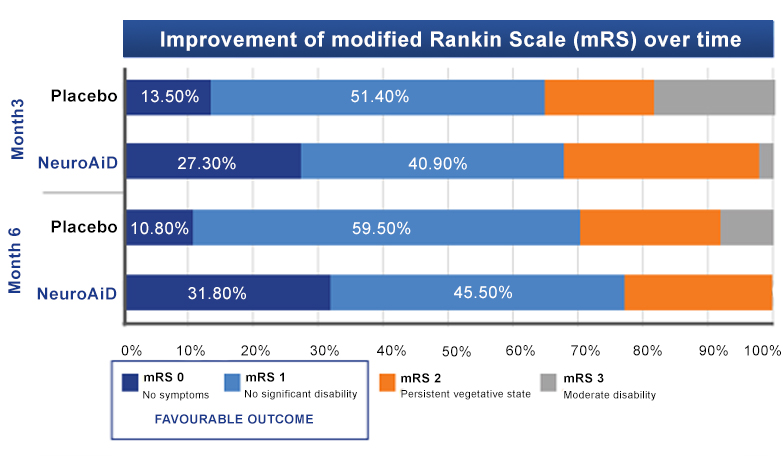
NeuroAiD tối ưu hóa khả năng phục hồi của các đối tượng TBI vừa và nặng theo thời gian
Truy cập tab Ấn bản
để biết thêm thông tin về dữ liệu lâm sàng của NeuroAiD
Cho đến nay, không có tương tác thuốc nào với NeuroAiD được báo cáo. Nên dùng NeuroAiD cùng với các phương pháp điều trị phòng ngừa các yếu tố nguy cơ tim mạch thường được chỉ định sau đột quỵ; những loại thuốc này thường bao gồm thuốc chống kết tập tiểu cầu, thuốc hạ huyết áp và thuốc hạ cholesterol, trong số những loại thuốc khác như thuốc chống tiểu đường. Các thử nghiệm lâm sàng có hệ thống đã chỉ ra rằng NeuroAiD không có bất kỳ tương tác nào với aspirin. Bệnh nhân dùng NeuroAiD cùng với thuốc chống đông máu đã báo cáo rằng không có tác động nào đến INR (Tỷ lệ chuẩn hóa quốc tế) của họ. Tuy nhiên, nên tiếp tục theo dõi INR khi bắt đầu sử dụng NeuroAiD vì nó được thực hiện thường quy cho bệnh nhân dùng thuốc chống đông máu.
NeuroAiD được sản xuất tại Singapore theo tiêu chuẩn quốc tế về Thực hành sản xuất tốt (GMP). Các tiêu chuẩn GMP được áp dụng cho các quy trình sản xuất thực phẩm bổ sung, bao gồm phê duyệt nguyên liệu thô, kiểm soát quy trình và sản xuất, thử nghiệm trong phòng thí nghiệm cũng như đóng gói, dán nhãn và phân phối sản phẩm. Các quy trình này thường xuyên được kiểm toán bởi các cơ quan y tế độc lập. Mỗi lô NeuroAiD đều được phân tích kỹ lưỡng bởi các phòng thí nghiệm độc lập của bên thứ ba để xác nhận việc tuân thủ các tiêu chuẩn quốc tế, đảm bảo an toàn tối đa cho việc sử dụng NeuroAiD.
References:
2. PHÁT SINH THẦN KINH¹²
3. TẠO MẠCH³
4. ĐIỀU CHẾ VIÊM THẦN KINH⁴
BDNF là một yếu tố tăng trưởng điều chỉnh sự tồn tại của tế bào thần kinh và bảo vệ tế bào thần kinh khỏi những tổn thương do glutamate gây ra. BDNF cũng khuyến khích sự phát triển và biệt hóa của các tế bào thần kinh mới.
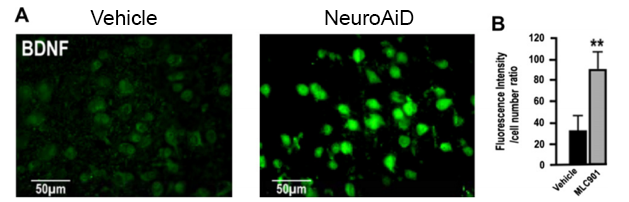
Tác dụng in vivo của tiền xử lý NeuroAiD đối với mức protein BDNF trong các phần vỏ não. ( A ) Các bức ảnh kính hiển vi phát quang đại diện cho biểu hiện miễn dịch BDNF ở các tế bào thần kinh vỏ não trong các phần não. ( B ) Định lượng cường độ tín hiệu BDNF trong các tế bào thần kinh được miễn dịch.
Kính hiển vi phát huỳnh quang đã xác nhận sự phát triển của mạng lưới sợi trục và đuôi gai quan trọng trên môi trường nuôi cấy tế bào với NeuroAiD.
Vào ngày 14, trong môi trường nuôi cấy tế bào thần kinh được điều trị bằng NeuroAiD, sự phát huỳnh quang cho thấy sự gia tăng đáng kể các biểu hiện DCX, GAP43 và Synaptotagmin, cung cấp bằng chứng cho thấy NeuroAiD kích hoạt:
NeuroAiD thúc đẩy cả sự phát triển của các kết nối khớp thần kinh mới và sửa đổi các kết nối hiện có, bao gồm cả việc tăng số lượng và độ dài của đuôi gai và khớp thần kinh. Chiều dài của tế bào thần kinh tăng 60% đã được thể hiện vào Ngày thứ 14 đối với nhóm NeuroAiD.
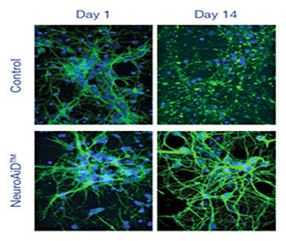
Tác dụng của điều trị MLC601/MLC901 đối với biểu hiện Synaptotagmin 1 trong ống nghiệm ở tế bào thần kinh vỏ não được nuôi cấy. Biểu hiện Synaptotagmin 1 được phân tích sau khi điều trị bằng MLC601/MLC901 (1 mg/ml) vào Ngày thứ 7 và 14 của quá trình điều trị.
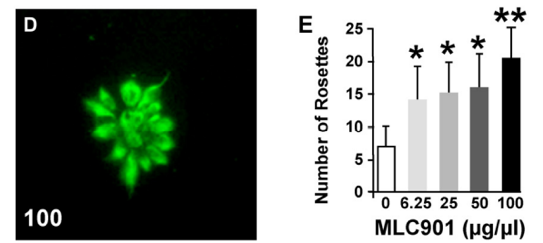
Tác dụng thần kinh của MLC901 đối với các tổ tiên có nguồn gốc từ ESC của con người. (D) Các tập hợp hình hoa thị rạng rỡ của các tế bào tiền thân thần kinh dương tính với Nestin hình thành một cách tự nhiên trong môi trường nuôi cấy mật độ thấp. (E) Định lượng số lượng hoa hồng 2 ngày sau khi bổ sung MLC901 (*P <0,05, **P <0,01 so với đối chứng).
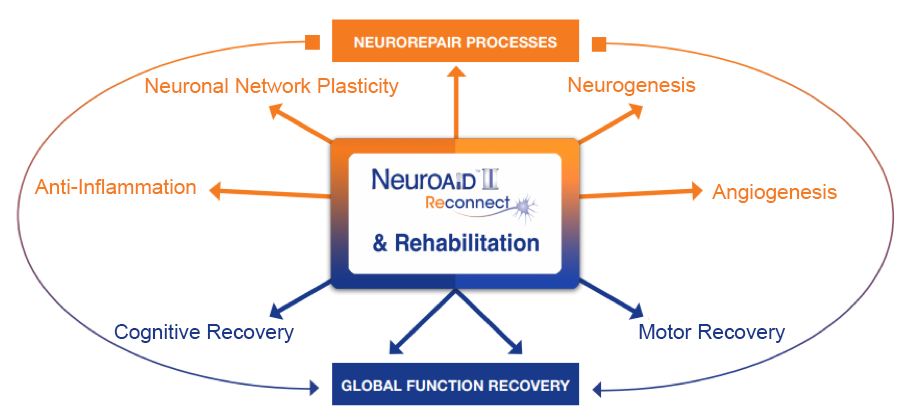
Truy cập tab Ấn phẩm để biết thêm thông tin về các thuộc tính và phương thức hoạt động của NeuroAiD.
References:
Bệnh Alzheimer (AD) là kết quả của một quá trình thoái hóa thần kinh liên quan đến nhiều nguyên nhân khác nhau và liên quan đến một số con đường dược lý. Với cơ chế hoạt động đa phương thức, NeuroAiD cung cấp một cách tiếp cận sáng tạo để điều trị bệnh Alzheimer.
NeuroAiD có một phương thức hoạt động đa phương thức dựa trên các đặc điểm nổi bật của cơ chế Bệnh Alzheimer.
Trong các điều kiện bệnh lý như AD, quá trình xử lý amyloidogen của protein tiền chất amyloid (APP) dẫn đến một lượng lớn các mảnh Aβ không hòa tan và gây độc thần kinh, gây ra sự hình thành các đám rối sợi thần kinh. Một phương pháp trị liệu sẽ nhắm mục tiêu xử lý APP để hạn chế con đường tạo amyloidogen.
Một nghiên cứu trong ống nghiệm được tiến hành trên môi trường nuôi cấy tế bào u nguyên bào thần kinh ở người cho thấy tác dụng của NeuroAiD đối với quá trình xử lý APP 1.
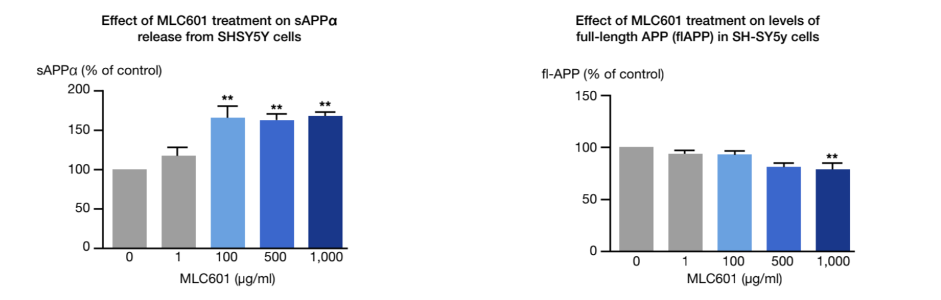
Quá trình phosphoryl hóa protein tau là một dấu hiệu bệnh học thần kinh khác của AD. Một nghiên cứu in-vivo cho thấy NeuroAiD đang tác động đến quá trình này 2.

AT8: kháng thể đơn dòng được sử dụng trong phương pháp làm mờ phương Tây để đo mức độ phosphoryl hóa tau
PHF: dây tóc xoắn ốc được ghép nối được sử dụng trong phương pháp làm mờ phương Tây để đo mức độ phosphoryl hóa tau
Nghiên cứu ATHENE 3
Một thử nghiệm ngẫu nhiên, mù đôi, có đối chứng với giả dược được tiến hành trên 125 đối tượng có thể mắc AD từ nhẹ đến trung bình, nhận NeuroAiD (MLC901, 2 viên, 3 lần một ngày) hoặc giả dược như một liệu pháp bổ sung cho điều trị AD tiêu chuẩn cho 6 tháng, sau đó là một nghiên cứu mở rộng có nhãn mở trong đó tất cả các đối tượng nhận được NeuroAiD bên cạnh tiêu chuẩn chăm sóc.
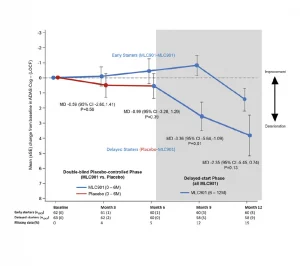
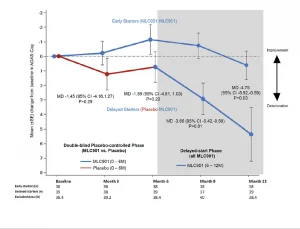
Nghiên cứu thí điểm nhãn mở bao gồm 124 bệnh nhân mắc bệnh Alzheimer không đạt được lợi ích từ đợt điều trị Rivastigmine 6 tháng trước đó (thiếu hiệu quả và/hoặc khả năng dung nạp kém), được điều trị bằng NeuroAiD trong 4 năm. Trạng thái nhận thức của các đối tượng được MMSE và ADAS-Cog đánh giá 6 tháng một lần.4*,5*
Trong một thử nghiệm đa trung tâm, ngẫu nhiên, có kiểm soát được tiến hành trên 264 bệnh nhân mắc bệnh Alzheimer nhẹ đến trung bình, NeuroAiD được so sánh với 3 chất ức chế cholinesterase đã được phê duyệt (tức là Donepezil, Rivastigmine, Galantamine) trong 16 tháng.6*
References
* Các nghiên cứu được tiến hành với NeuroAiD MLC601 với liều 1 viên, 3 lần một ngày.
NeuroAiDTM là thương hiệu của Moleac. MLC601 (NeuroAiDTM) và MLC901 (NeuroAiDTTMI/ NurAiDTTMI) là hai công thức độc quyền khác nhau đã được chứng minh là tương đương về mặt dược lý học và được gọi là “NeuroAiD” trong tài liệu này.
Moleac đã phát triển nhiều quan hệ đối tác với các công ty có cùng giá trị và tầm nhìn để cung cấp các giải pháp sáng tạo ở từng thị trường và giải quyết các nhu cầu y tế chưa được đáp ứng, đặc biệt là phục hồi sau đột quỵ và chấn thương sọ não.
Mạng lưới đối tác ngày càng phát triển của chúng tôi đảm bảo cung cấp NeuroAiD cho số lượng lớn hơn nữa nạn nhân đột quỵ và nạn nhân bị chấn thương sọ não trên toàn thế giới cũng như những bệnh nhân bị suy giảm nhận thức.
Kể từ năm 2006, NeuroAiD đã mở rộng sự hiện diện của mình tại hơn 32 quốc gia và chúng tôi vẫn đặt mục tiêu cung cấp NeuroAiD cho nhiều bệnh nhân có nhu cầu hơn trên toàn thế giới.
 Văn phòng
Văn phòng Đối tác
Đối tác